H2O2有强氧化性,而I-具有强还原性,它们在酸性条件发生氧化还原反应。
离子方程式: H2O2 + 2I- + 2H+ = I2 + 2H2O
过氧化氢要分解成水和氧气,过氧化氢里面的两个氧要由1价便成1个0价(氧气),1个1价(水中的氧)。
+3价的铁离子有强氧化性,可以先从1个氧中得到1个电子便成+2价的亚铁离子,让1价的氧原子便成氧气(跑掉),然后再失去1个电子(变成+3价铁离子)。
让1价的氧变成水份子中⑵价更稳定的氧离子。这也就是+3价铁离子的催化作用。
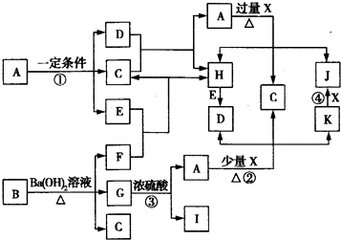
碘化钾发生还原反应的其他实例:
1、碘离子I−可被强氧化剂如氯气等氧化为I2单质:
2 KI(aq) + Cl2(aq)→ 2 KCl + I2(aq)
该反应可用于天然产物当中提取碘,也可验证氯气的存在。
空气也可以氧化碘离子,当KI样品长期放置后用二氯甲烷淋洗可以发现萃取层的颜色为紫色(碘单质溶于有机溶剂的颜色)。当处于酸性环境中,氢碘酸(HI)是一种强还原剂。
2、碘化钾还可将浓硫酸直接还原为硫化氢:
8KI+9H2SO4→(KHSO4)8·4H2O+4I2+H2S [3]
3、如同其他的碘盐,KI和单质碘反应可以形成I3−:
KI(aq) + I2(s) → KI3(aq)
不同于I2,I3−盐易溶于水,并且可以通过该反应使碘用于氧化还原滴定。KI3水溶液,即“Lugol溶液”,可用于消毒剂和黄金表面的腐蚀剂。
百度百科-碘化钾
百度百科-过氧化氢(双氧水)
百度百科-氧化还原反应